
FDA autoriza la primera prueba de aliento para detectar el COVID-19
El nuevo dispositivo puede otorgar resultados en menos de tres minutos y su sistema separa e identifica mezclas químicas para detectar cinco compuestos asociados con la infección por SARS-CoV-2.
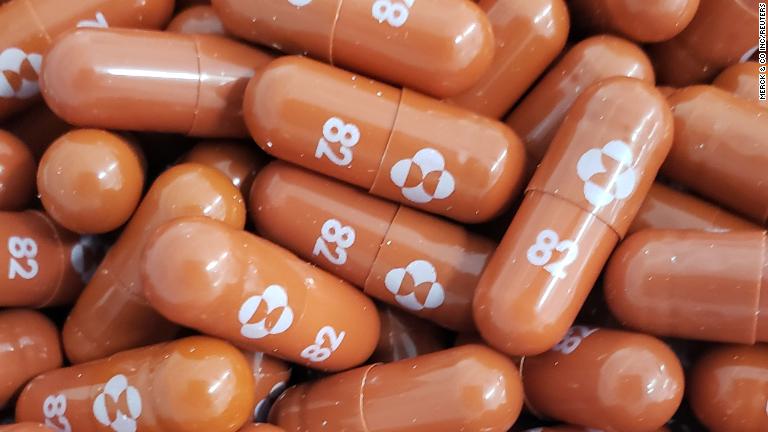
FDA autorizó el uso de emergencia para la píldora contra el COVID-19 de Merck
La Administración de Alimentos y Medicamentos de Estados Unidos otorgó el permiso para el uso de la píldora antiviral molnupiravir, para los "adultos con resultados positivos en las pruebas virales directas de SARS-CoV-2, y que tienen un alto riesgo de progresión a COVID-19 grave, incluyendo la hospitalización o la muerte".

Paxlovid de Pfizer: La FDA autoriza el primer antiviral oral contra el COVID-19
El tratamiento consiste en una píldora que puede tomarse en casa antes de que las personas se enfermen lo suficiente como para necesitar hospitalización, entre los primeros tres a cinco días de presentar síntomas de la enfermedad. El tratamiento reduce el riesgo de hospitalización o muerte en un 89%.
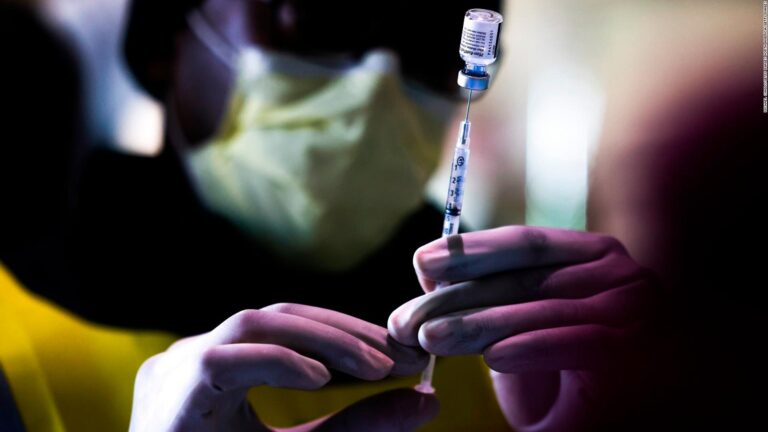
La FDA autorizó refuerzo de las vacunas de Pfizer y Moderna para todos los adultos
Las empresas solicitaron la autorización para los refuerzos la semana pasada con base en los resultados de un ensayo de fase 3 que involucró a más de 10.000 participantes y encontró que los refuerzos eran seguros y tenían una eficacia del 95% contra el COVID-19.
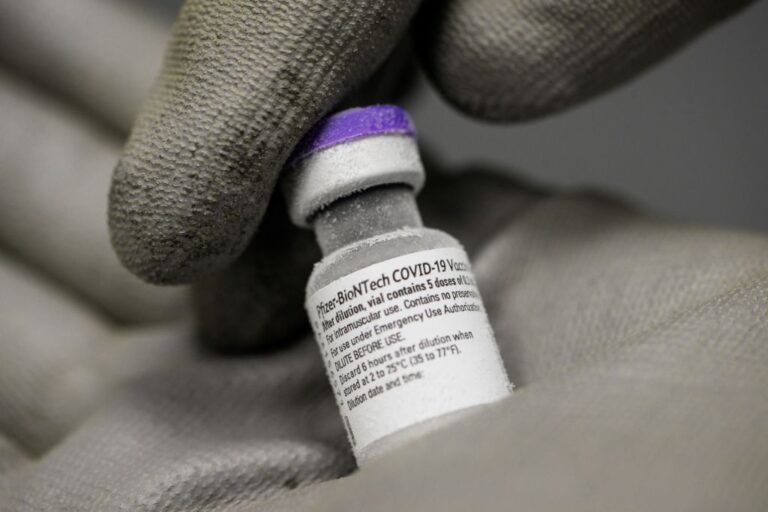
COVID-19: FDA autoriza refuerzo de las vacunas de Pfizer y Moderna para todos los adultos
Las farmacéuticas solicitaron la autorización la semana pasada basándose en los resultados de un ensayo de fase 3 que involucró a más de 10 mil participantes. “Autorizar el uso de una sola dosis de refuerzo (...) ayuda a brindar protección continua contra el COVID-19”, dijeron desde las FDA.

Pfizer busca que la FDA autorice dosis de refuerzo para todos los adultos
Las empresas dijeron que la solicitud se basa en los resultados de un ensayo de fase 3 que incluyó a más de 10.000 participantes, donde se comprobó que las dosis de refuerzo eran seguras y tenían una eficacia del 95% contra el COVID-19 sintomático en comparación con el esquema de dos dosis de la vacuna en el período en que la variante Delta, fuertemente contagiosa, era la dominante.
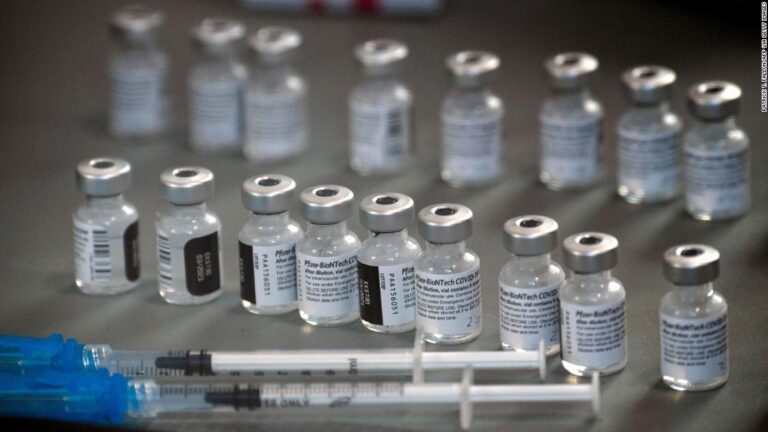
COVID-19: FDA autorizó el uso de emergencia de la vacuna de Pfizer para niños entre 5 a 11 años
El debate ahora pasará al Comité Asesor sobre Prácticas de Inmunización que se reunirá el 2 de noviembre para discutir si recomiendan el uso de la vacuna entre los niños estadounidenses. Hasta la fecha las dosis de Pfizer cuentan con autorización para administrarse en menores entre 12 y 15 años.
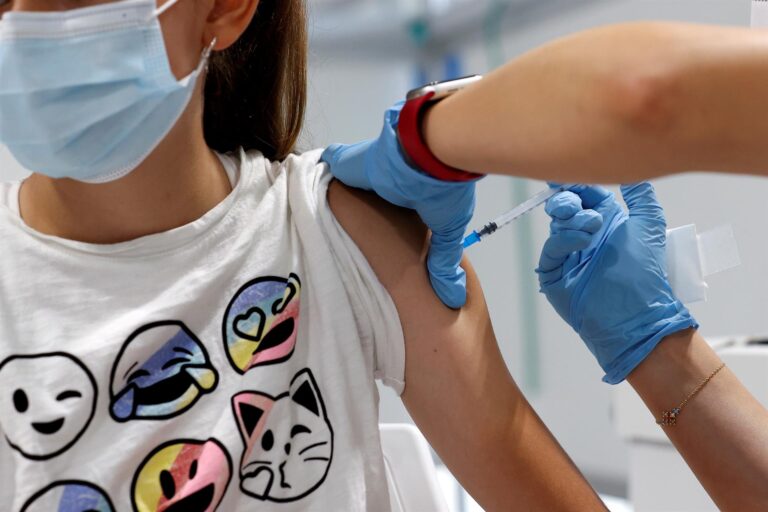
Asesores de la FDA recomiendan vacunación a niños entre 5 y 11 años con Pfizer
La FDA había dicho que en la mayoría de los escenarios que proyectaba, los beneficios de vacunar a los niños más pequeños superarían cualquier riesgo. Además, Pfizer señaló que los ensayos clínicos mostraron que la vacuna era más del 90% efectiva para prevenir la infección sintomática en los niños.

FDA planea autorizar la combinación de vacunas como dosis de refuerzo contra el COVID-19
La Administración de Alimentos y Medicamentos de Estados Unidos ya ha autorizado refuerzos para la vacuna Pfizer y actualmente está considerando la autorización para las vacunas Moderna y Johnson & Johnson. Aunque los detalles siguen sin estar claros, se espera que hagan una autorización amplia sobre mezclar y combinar potencialmente tan pronto como esta semana.
Asesores de la FDA votan unánimemente para recomendar dosis de refuerzo de la vacuna J&J en mayores de 18 años
El Comité Asesor de Vacunas y Productos Biológicos Relacionados respaldó categóricamente en una votación de 19-0, las vacunas para todos los receptores de vacunas de J&J en mayores de 18 años, al menos dos meses después de su primera dosis. El siguiente paso es que la FDA considere la recomendación.

La primera autorización de este producto: FDA aprobó la venta de los cigarrillos electrónicos Vuse
La Administración de Alimentos y Medicamentos (FDA) de Estados Unidos informó este martes que autorizó a R.J. Reynolds para vender tres de sus productos de vapeo. "Si bien la acción de hoy permite que los productos de tabaco se vendan en Estados Unidos, esto no significa que sean seguros o estén aprobados por la FDA", explicaron en un comunicado.

Merck pide a la FDA autorización de uso de emergencia para el molnupiravir, el antiviral experimental contra el COVID-19
Si la FDA aprueba el uso de emergencia del medicamento, se convertiría en el primer tratamiento oral para combatir el COVID-19. El fabricante señaló que ofrecerá precios escalonados para facilitar el acceso en todo el mundo y que espera producir 10 millones de tratamientos para finales de 2021.
Lo más leído
- Tras quiebre previo a votación de proyecto de reconstrucción: Parisi se reunirá con el ministro Quiroz
- Pedro Araya acusa “mal manejo” del Gobierno por caída de acuerdo con el PDG: “Se le están descolgando aliados”
- “En las condiciones que nos entregaron el avance, era imposible”: PDG explica quiebre de acuerdo por megarreforma
- Tras operativo en Temucuicui: Solo uno de los detenidos quedó en prisión preventiva
- “Cuando duermes con niños, amaneces mojado”: Hoffmann aborda presión del PDG al Gobierno